Les Salmonidés dans les lacs de montagne français
Dans la plupart des lacs de montagne, des Salmonidés ont été introduits et se sont établis de manière pérenne. La diversité des contextes environnementaux de ces lacs induit des différences notables dans leurs morphologies et les ressources qu’ils consomment. La prise en compte des contraintes environnementales pourrait orienter les futures politiques de gestion de ces espèces dans ces écosystèmes soumis aux changements environnementaux.
Des enjeux d’actualité
Depuis des siècles, les Salmonidés ont commencé à être introduits dans de nombreux lacs de montagne pour des raisons d’alimentation et cette pratique s’est fortement intensifiée au cours de la seconde moitié du vingtième siècle pour soutenir le développement de la pêche de loisir (Knapp et Matthews, 2000 ; Ventura et al., 2017 ; Loheac et al., 2019 ; Fagín et al., 2025). La question de leur impact sur la biodiversité s’est rapidement posée et différentes études ont montré des effets significatifs sur le zooplancton, les invertébrés benthiques et les amphibiens (Knapp et Matthews, 2000 ; Tiberti et al., 2014 ; Milardi et al., 2016 ; Miró et al., 2020). Actuellement, la question du maintien des populations de Salmonidés dans ces écosystèmes originellement apiscicoles se pose aux gestionnaires pour deux raisons principales. Premièrement, le souhait d’une reconquête de naturalité (wilderness) (Knapp et al., 2001) peut motiver la volonté d’éradiquer les Salmonidés perçus comme des marqueurs d’anthropisation dans des écosystèmes généralement considérés comme préservés. Deuxièmement, les lacs d’altitude sont souvent localisés dans des zones naturelles protégées comprenant la présence d’espèces d’intérêt pour la conservation et vulnérables à la prédation des Salmonidés (par exemple, le calotriton des Pyrénées – Calotriton asper, directive Habitats annexe II) ou le triton alpestre – Triturus alpestris, directive Habitats annexe IV).
Dans ce contexte, notre étude a été menée non pas pour estimer un impact des Salmonidés sur la biodiversité des lacs, puisque de nombreux travaux ont déjà été menés sur cette question, mais plutôt pour mieux comprendre les déterminants qui affectent leurs conditions de vie et l’origine des ressources alimentaires soutenant ces populations. Nos investigations apportent ainsi de nouvelles connaissances concernant l’écologie des Salmonidés dans ces milieux d’altitude et pourront contribuer aux débats actuels concernant leurs gestions futures en considérant à la fois les enjeux halieutiques et ceux de conservation. Pour répondre à nos questions, nous avons considéré neuf lacs hébergeant des populations naturalisées (capables de se reproduire et de se maintenir de façon autonome) d’omble chevalier (Salvelinus alpinus) et de cristivomer (Salvelinus namaycush) afin que nos résultats ne soient pas affectés par des introductions piscicoles récentes.
Condition de vie
La première interrogation concernant la présence des Salmonidés dans les milieux de montagne est généralement en lien avec leur capacité de survie dans ces environnements extrêmes, particulièrement du point de vue thermique. Bien que les Salmonidés soient généralement considérés comme sténothermes
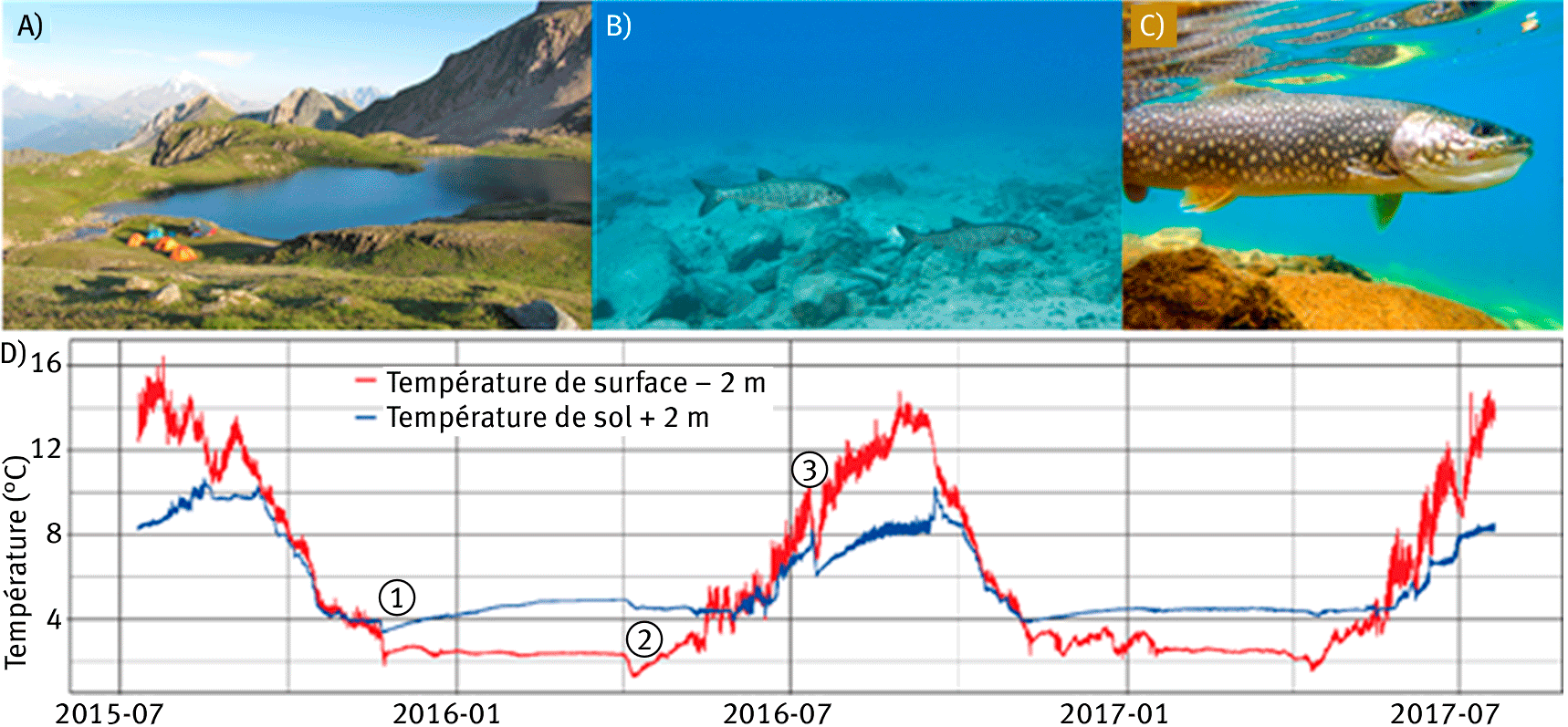
Figure 1. (A) Lac de la Forclaz (2 471 m), typique des lacs d’altitude formés par une dépression issue du retrait glaciaire. Le campement est installé au bord du lac et permet à l’équipe scientifique d’effectuer l’ensemble des investigations de terrain sur plusieurs jours. (B) Jeunes cristivomers issus d’une population naturalisée dans le lac Pépin (2 728 m). L’habitat aquatique est très minéral et la transparence de l’eau reflète les faibles concentrations en nutriments présents dans l’eau (oligotrophie). (C) Les cristivomers adultes peuvent atteindre des tailles de plus de 60 cm, mais certains individus peuvent approcher le mètre et vivre plusieurs décennies. (D) La température est une variable environnementale particulièrement contraignante pour le développement des Salmonidés dans ces milieux d’altitude avec des effets sur leur métabolisme mais aussi sur la disponibilité en ressources. Les enregistrements thermiques, ici lac du Lou (2 035 m), montrent que l’englacement de la surface du lac se produit dès fin novembre (1) et se termine fin avril (2) avec une diminution momentanée de la température des eaux de surface dûe à la fonte de la glace. On note aussi la présence de chute momentanée de température affectant à la fois les eaux de surface et de fond en lien avec des événements météorologiques locaux (3)
Équation 1
Coefficient de Fulton = (Poids (g) / Taille3 (mm)) ×100
Nous avons donc préféré retenir le coefficient de condition spécifique (Kn, équation 2 ; Peig et Green, 2010) qui prend en compte à la fois les différences interspécifiques intrinsèques et les changements morphologiques pouvant survenir au cours de l’ontogénie des individus. Ce coefficient représente un ratio informant de la déviation entre le poids observé d’un individu par rapport au poids attendu selon sa taille obtenu d’après les données de l’ensemble de populations de la même espèce, ici les populations présentes dans les différents lacs (droites de la figure 2A). Son interprétation est la même que pour le coefficient de Fulton (bonne condition pour Kn > 1).
Équation 2
Coefficient relatif (Kn) = Poids (g) / (a×Tailleb (mm))
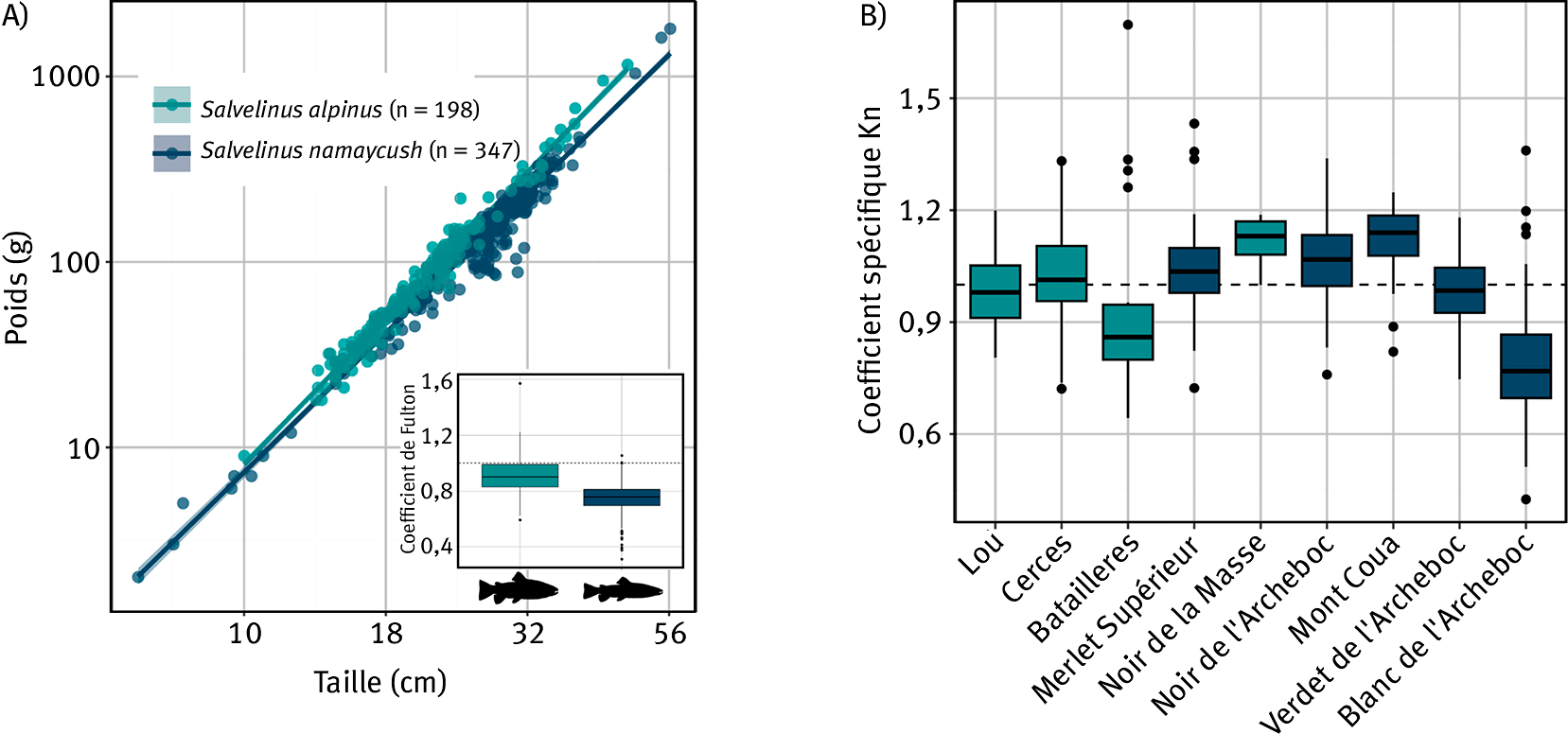
Figure 2. (A) Relation (log-log) entre la taille et le poids des Salmonidés capturés dans les neuf lacs étudiés. L’insert montre le coefficient de Fulton qui présente des variations significatives entre espèces distinguant les différentes morphologies suggérées par les icônes. (B) Le coefficient relatif Kn permet de s’affranchir des différences morphologiques spécifiques et met en évidence des différences de conditions entre lacs pour les deux espèces. Les lacs sont ordonnés par altitude croissante de gauche à droite.
Les conditions spécifiques varient significativement entre lacs pour les deux espèces (tests de Kruskal-wallis, p > 0,001). Cela suggère que certains lacs sont plus propices à la bonne condition corporelle des poissons que d’autres. Par exemple, dans le lac du Mont Coua, les cristivomers présentent un poids supérieur à celui attendu (Kn > 1) suggérant des conditions de vie favorables malgré l’altitude importante du lac (2 672 m) comme l’avait reporté Martinot (1978) à la différence du lac Blanc de l’Archeboc (2 850 m) où les conditions spécifiques des cristivomers sont relativement dégradées (Kn moyen = 0,8) comme préalablement reportés par Loheac (2020b).
L’altitude est un facteur affectant significativement la condition spécifique pour le cristivomer (ANOVA, p < 0,001) mais pas pour l’omble chevalier (ANOVA, p = 0,16) (figure 3A). Cependant, on peut noter que l’omble chevalier n’est présent dans les lacs étudiés que jusqu’à ~ 2 500 m et est ensuite remplacé par le cristivomer. Cette transition de peuplement piscicole à ~ 2 500 m peut être en lien avec les conditions de vie particulièrement contraignantes au-delà de cette altitude pour l’omble chevalier, menant à des politiques d’introduction variables en adéquation avec l’écologie des espèces. En se focalisant sur le cristivomer, un modèle linéaire multiple permet d’expliquer une fraction non négligeable des variations de conditions spécifiques (ANOVA, p < 0,001, R2adj = 0,35 ; figure 3B). Les effets partiels représentés permettent d’isoler l’impact spécifique de chaque variable sur la condition spécifique du cristivomer, en contrôlant l’influence des autres variables du modèle. Il ressort ainsi que la profondeur à un effet négatif dominant sur la dégradation du coefficient spécifique qui est contrebalancé positivement lorsque les températures de l’eau sont plus chaudes et les invertébrés (c’est-à-dire la ressource alimentaire) plus abondants. Les conditions spécifiques dégradées des cristivomers dans le lac Blanc de l’Archeboc peuvent ainsi s’expliquer par une forte profondeur (42 m), des températures hivernales faibles (~ 1,1 °C) et une ressource en invertébrés limitée (~ 250 ind m²). À l’inverse, le lac du Mont Coua, bien que présentant des températures hivernales similaires (~ 1,4 °C), bénéficie d’une faible profondeur (10 m) et de fortes densités d’invertébrés littoraux (~ 6 250 ind m²) permettant aux cristivomer présents dans ce lac d’atteindre de bonnes conditions spécifiques.
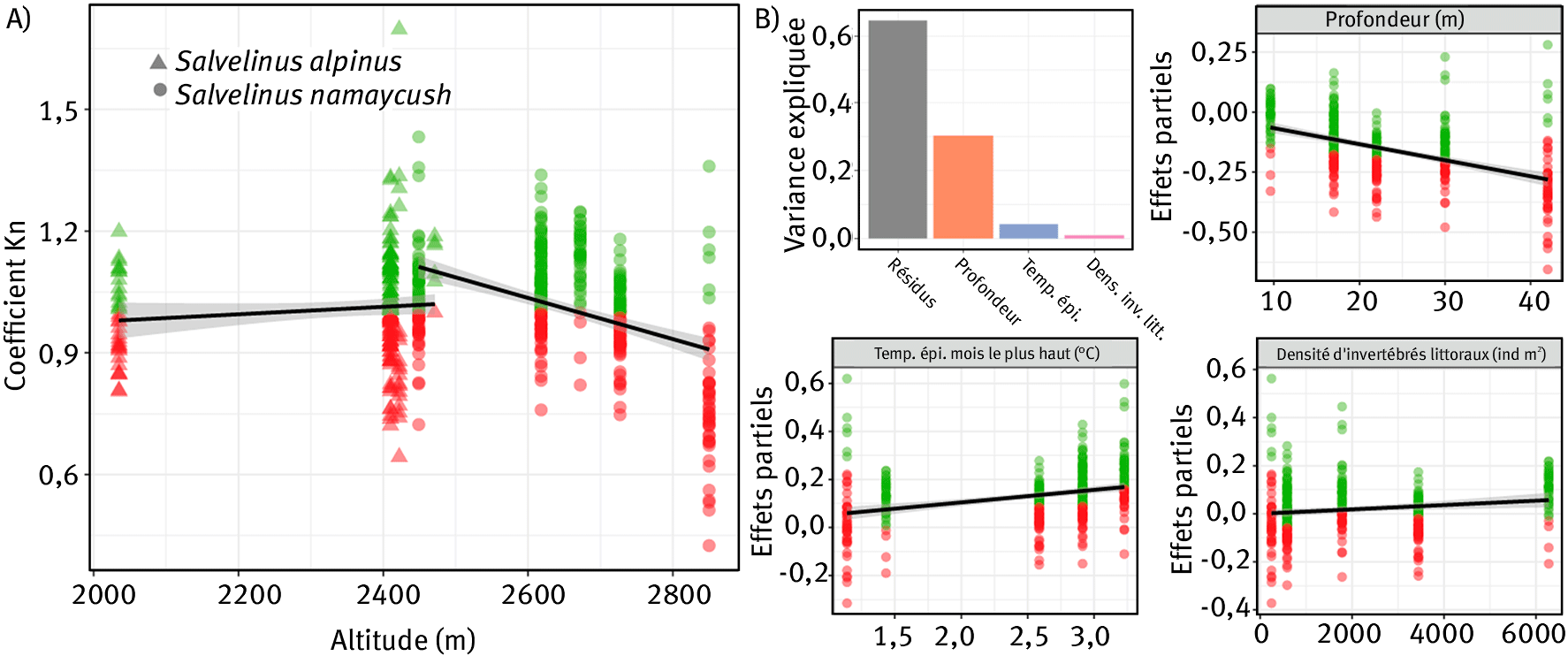
Figure 3. (A) Variations du coefficient spécifique Kn en fonction de l’altitude pour l’omble chevalier et pour le cristivomer. (B) Effets partiels des trois variables retenues dans le modèle linéaire multiple permettant d’expliquer les variations de coefficients spécifiques pour le cristivomer. Les individus en vert ont de bonnes conditions individuelles (coefficients spécifiques supérieurs à 1) et ceux en rouge présentent des conditions individuelles altérées (coefficients spécifiques inférieurs à 1).
Ressources utilisées
Les Salmonidés sont opportunistes et peuvent consommer à la fois des proies aquatiques et terrestres, en particulier dans les écosystèmes d’altitude (Mann et al., 1989 ; Cavalli, 1997 ; Horká et al., 2017). Afin d’identifier les ressources que ceux-ci utilisaient dans les lacs étudiés, nous avons eu recours à une approche basée sur l’analyse comparée des compositions isotopiques (carbone et azote) des tissus des poissons et de leurs ressources possibles. Cette approche est largement utilisée en écologie et possède l’avantage, comparativement à l’analyse des contenus stomacaux, de fournir une estimation intégrée au cours de la vie du poisson des ressources assimilées par les consommateurs. L’estimation des contributions relatives de chaque ressource utilisée pour chaque individu a pu ainsi être quantifiée par le biais de modèles de mélange Bayésien (Parnell et al., 2010 ; Phillips et al., 2014).
Nos résultats mettent en évidence que les Salmonidés consomment majoritairement des ressources issues de la zone littorale des lacs (figure 4). La consommation de ressources benthiques des zones profondes et pélagiques apparaissent très minoritaires bien que la consommation de zooplancton (ressources pélagiques) ait été reportée par ailleurs (Eloranta et al., 2013). La contribution minoritaire du zooplancton dans le régime alimentaire des poissons pourrait s’expliquer par la taille moyenne relativement importante des poissons capturés (26,5 cm) pour lesquels le zooplancton pourrait être une proie énergétiquement peu profitable du fait de sa petite taille (quelques dixièmes de millimètres à quelques millimètres). Alternativement, la prédation par les Salmonidés pourrait avoir induit la disparition du zooplancton de grande taille (Daphnia sp.) ou son maintien à des densités faibles dans certains lacs ne permettant donc plus que cette ressource constitue une contribution majeure à leur régime alimentaire.
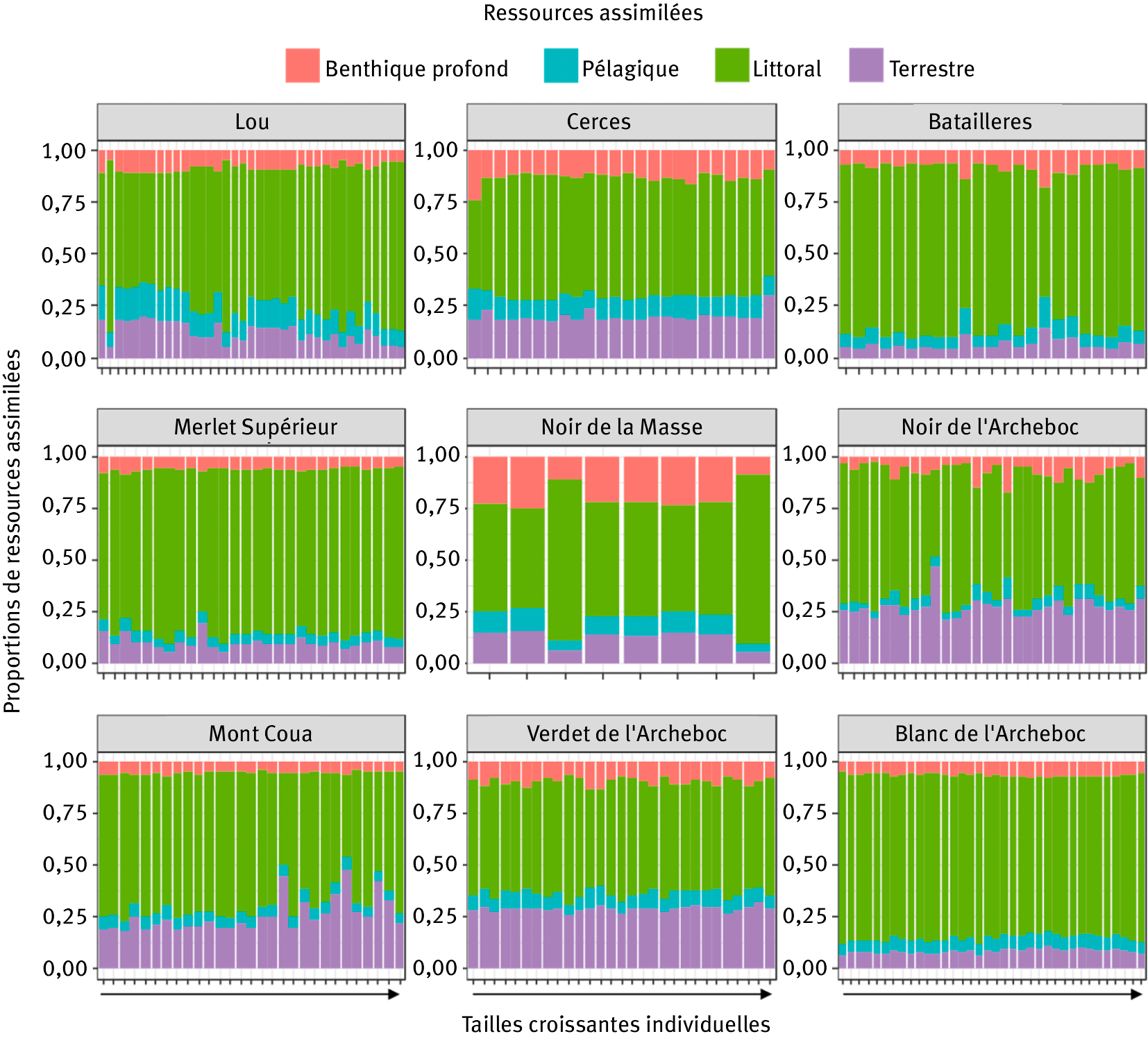
Figure 4. Ressources utilisées par les Salmonidés dans les neuf lacs étudiés estimées par un modèle de mélange Bayésien d’après les compositions isotopiques en carbone et en azote des Salmonidés et de leurs ressources. Les Salmonidés sont ordonnés par ordre croissant de taille de gauche à droite.
Si aucune variation significative dans les ressources utilisées n’est identifiée avec la taille des individus (ANOVA, p > 0,05), des variations significatives des proportions de ressources terrestres existent entre lacs (test de Kruskal-Wallis, p < 0,001), variant de 6,5 % pour le lac de Bataillières à 28,9 % pour le lac Verdet de l’Archeboc. Les variations de la consommation des ressources terrestres par les Salmonidés semblent ainsi représenter une caractéristique majeure distinguant les régimes alimentaires des populations étudiées entre les différents lacs.
En conduisant la même approche que pour les coefficients spécifiques, nous avons mis en évidence que l’utilisation de ressources terrestres augmente avec l’altitude, bien qu’une forte variabilité entre et au sein des lacs existe (R2ad = 0,04 ; p = 0,002, figure 5A). D’ailleurs, pour le lac le plus en altitude (lac Blanc de l’Archeboc, 2 850 m), les ressources terrestres utilisées sont particulièrement faibles (8,5 %). La prise en compte des caractéristiques intrinsèques aux lacs permet finalement d’expliquer une part substantielle de la variation de l’utilisation des ressources terrestres par les Salmonidés en considérant trois variables (R2ad = 0,35 ; p < 0,001, figure 5B). La superficie des lacs a un effet majeur sur l’utilisation de cette ressource, suivie de la profondeur et des températures estivales. Ainsi, plus le lac est grand et profond, moins il est probable que les Salmonidés se nourrissent de proies terrestres. Ce résultat met en évidence un effet de dilution des ressources terrestres disponibles pour les écosystèmes de grande taille. En effet, le ratio périmètre des berges (d’où proviennent les ressources terrestres) sur surface du lac (ou volume associé à la profondeur) diminue avec la taille du lac. On observe également que plus les températures estivales sont chaudes, moins la proportion de proies terrestres assimilées est importante. L’effet négatif des températures estivales pourrait être une résultante indirecte de la contrainte thermique sur la production d’invertébrés aquatiques ; plus les températures estivales de l’eau sont froides plus la production d’invertébrés aquatiques sera faible et les Salmonidés se tourneraient ainsi plus vers les ressources terrestres.
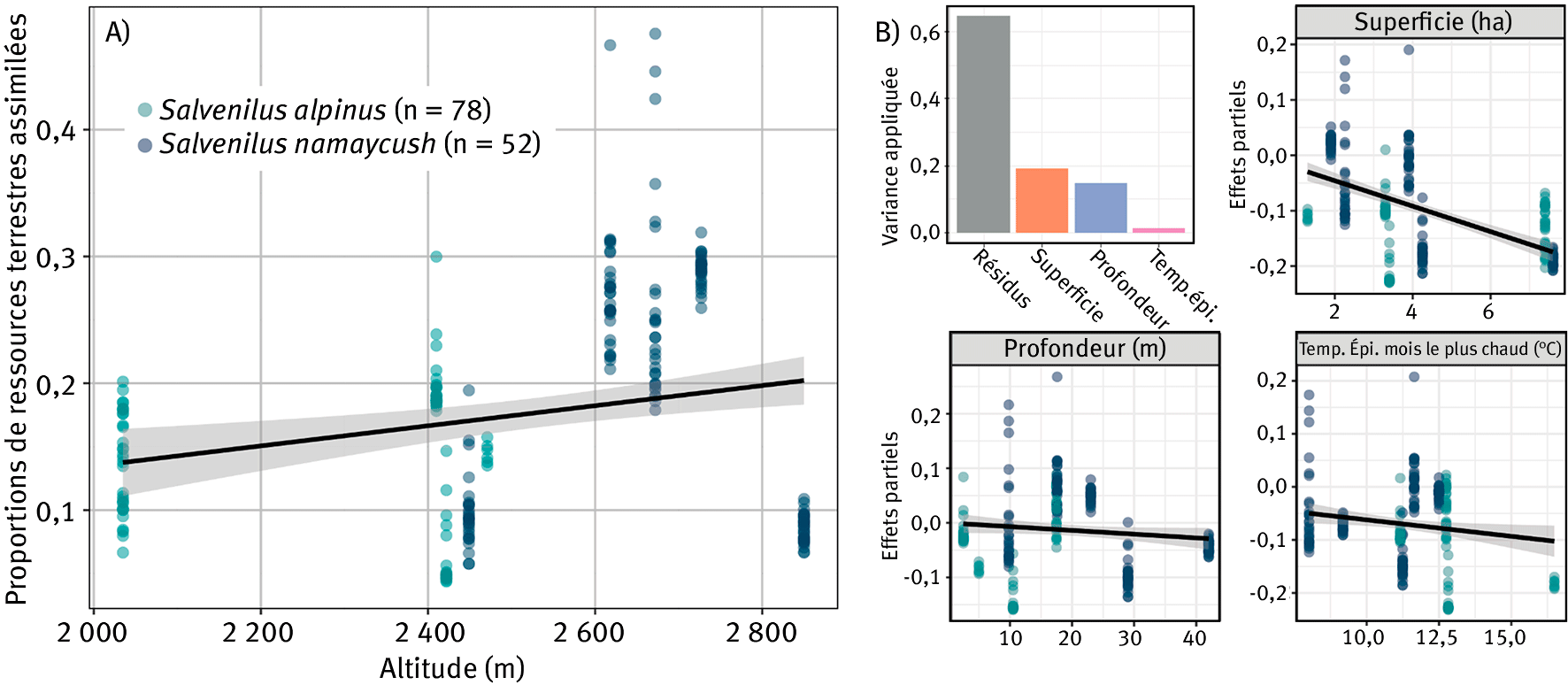
Figure 5. Changement de la proportion de ressources terrestres assimilées par les Salmonidés en fonction de l’altitude (A). Effets partiels des trois variables retenues dans le modèle linéaire multiple permettant d’expliquer les variations de proportions de ressources terrestres assimilées par les Salmonidés (B).
Synthèse et perspectives
Nos résultats ont montré que les conditions de vie entre lacs d’altitude différent et ne deviennent véritablement contraignantes pour la survie des Salmonidés qu’au-delà de 2 700 m pour le cristivomer. Bien que cette espèce puisse se maintenir dans une large gamme de contextes écologiques, les environnements les plus contraignants affectent leur bonne condition corporelle mettant en évidence des conditions de vie non optimales. Malgré tout, dans le lac Blanc de l’Archeboc, la population est naturalisée et pérenne depuis plus de trente ans (dernière introduction de juvéniles 0+ en 1993 ; Loheac, 2020a) malgré des conditions spécifiques dégradées, ce qui met en évidence les capacités de résistance de cette espèce vis-à-vis des conditions environnementales.
La morphologie lacustre (profondeur) et les conditions thermiques (température hivernale) expliquent les variations de condition des cristivomers et impliquent probablement un ensemble d’effets directs mais aussi indirects (Vagnon et al., 2023b). Par exemple, les températures froides affectent directement le métabolisme des individus mais influencent aussi la production de ressources. Les lacs peu profonds semblent ainsi les plus propices pour l’atteinte de bonnes conditions corporelles pour les cristivomers. Leurs conditions corporelles pourraient ainsi s’améliorer si les températures hivernales se réchauffent et dans la mesure où elles n’affectent pas la reproduction (maturation des gonades et incubation des œufs). Notons enfin qu’au sein de chaque lac, une forte variabilité de condition corporelle est rencontrée, probablement en lien avec des variations inter-individuelles qu’elles soient d’ordres métabolique, comportemental (par exemple, exploitation des habitats) ou trophique (piscivorie). Cette facette de l’écologie des individus au sein des populations de Salmonidés reste à explorer.
L’approche isotopique permet d’avoir une information intégrée dans le temps pour une évaluation à l’échelle de la saison de croissance des ressources utilisées par les Salmonidés dont les analyses détaillées de régimes alimentaires ont montré qu’elles variaient au cours de l’année (Cavalli,1997 ; Amundsen et al., 2010). La dominance de ressources littorales utilisées montre l’importance de la production aquatique pour le maintien des populations de Salmonidés dans ces lacs d’altitude. Les Chironomidae sont la famille d’invertébrés benthiques la plus diversifiée et la plus abondante dans les lacs étudiés (Loheac, 2020a) et représentent probablement les proies de prédilection des Salmonidés au sein de la zone littorale comme cela a été montré par analyses de contenus stomacaux de ces lacs (Martinot, 1978) ou dans d’autres (Cavalli, 1997).
L’augmentation de l’utilisation de ressources terrestres avec l’altitude souligne l’implication des apports terrestres comme substituts trophiques des proies aquatiques dont la production tendrait à diminuer avec l’altitude du fait de la diminution de température de l’eau. En effet, la faune d’invertébrés terrestres peut rester particulièrement abondante jusqu’à 3 000 m d’altitude (Caspers, 1970 ; Steinwandter et Seeber, 2023). Les caractéristiques morphologiques des lacs (profondeur et superficie) sont des caractéristiques propres à chaque système qui conditionnent l’utilisation des ressources terrestres avec une plus forte assimilation de ressources terrestres attendue dans les petits lacs peu profonds. La morphologie des lacs affecte ainsi à la fois les conditions corporelles des Salmonidés et l’utilisation de leurs ressources trophiques. Ces éléments pourraient contribuer à identifier les écosystèmes dans lesquels leur maintien ou leur établissement est le plus optimal.
Dans un contexte de réchauffement climatique, les conditions thermiques devraient devenir de plus en plus favorables aux Salmonidés dans les lacs d’altitude actuellement colonisés. D’un point de vue prospectif, le retrait glaciaire actuel a déjà permis l’apparition de nombreux nouveaux lacs (Mansoux et al., 2020) et leurs retraits futurs (Bosson et al., 2023) devraient induire l’apparition des dizaines de nouveaux lacs dans les Alpes (Cathala et al., 2021). La capacité de ces futurs écosystèmes à héberger des populations de Salmonidés pourrait, pour partie, être évaluée à l’aune des résultats obtenus et précédée d’un bilan des ressources trophiques disponibles (zooplancton et macroinvertébrés, aquatiques vs. terrestres) mais aussi de la biodiversité présente (par exemple, présence d’espèces protégées). La quantification des interactions écologiques directes et indirectes entre les Salmonidés et la biodiversité locale par le biais d’approches de réseaux trophiques par exemple (Vagnon et al., 2023a) pourrait constituer une voie de recherche prometteuse pour mieux comprendre leurs effets sur le fonctionnement lacustre.
Remerciements
Les auteurs remercient les co-financeurs de l’étude que sont le Parc naturel de la Vanoise, EDF, L’Agence de l’eau Rhône-Méditerranée-Corse et la Fédération nationale pour la pêche en France ainsi que l’ensemble des prestataires ayant participé à l’acquisition des données et particulièrement Sialis (prélèvements en plongée), Becq’eau (traitement des échantillons phytoplancton), Sage Environnement (traitement des échantillons IBL), Savoie Labo (analyses physico-chimiques), Téléos (pêches aux filets).
_______________________________________
Photo d’entête : Philippe Rogez - CC BY SA 4.0
Notes
- 1. Qui ne peut vivre que dans un milieu sujet à de faibles variations de température.
Références
- Amundsen, P., Knudsen, R., & Bryhni, H. T. (2010). Niche use and resource partitioning of Arctic charr, European whitefish and grayling in a subarctic lake. Hydrobiologia, 650(1), 3‑14. https://doi.org/10.1007/s10750-009-0054-9
- Bosson, J. B., Huss, M., Cauvy-Fraunié, S., Clément, J. C., Costes, G., Fischer, M., Poulenard, J., & Arthaud, F. (2023). Future emergence of new ecosystems caused by glacial retreat. Nature, 620(7974), 562‑569. https://doi.org/10.1038/s41586-023-06302-2
- Caspers, H. (1970). M. S. Mani : Ecology and Biogeography of High Altitude Insects. Series entomologica vol 4. The Hague : Dr. W. Junk N. V. Publ. 1968. XVI + 528 pp. D. Gl. 100, US $ 27.80. Internationale Revue Der Gesamten Hydrobiologie Und Hydrographie, 55(3), 501‑502. https://doi.org/10.1002/iroh.19700550332
- Cathala, M., Magnin, F., Linsbauer, A., & Haeberli, W. (2021). Modelling and characterizing glacier-bed overdeepenings as sites for potential future lakes in the deglaciating French Alps. Géomorphologie Relief Processus Environnement, 27(1), 19‑36. https://doi.org/10.4000/geomorphologie.15255
- Cavalli, L. (1997). Biologie des populations de Salmonidés des lacs de haute altitude du Parc National des Ecrins. Alimentation - Croissance - Reproduction [Thèse de doctorat. Université de Provence, Marseille].
- Eloranta, A. P., Knudsen, R., & Amundsen, P. (2013). Niche segregation of coexisting Arctic charr (Salvelinus alpinus) and brown trout (Salmo trutta) constrains food web coupling in subarctic lakes. Freshwater Biology, 58(1), 207‑221. https://doi.org/10.1111/fwb.12052
- Fagín, E., Felip, M., Brancelj, A., Masqué, P., & Catalan, J. (2025). Parasite sedimentary DNA reveals fish introduction into a European high-mountain lake by the seventh century. Nature Communications, 16(1), 3081. https://doi.org/10.1038/s41467-025-57801-x
- Horká, P., Sychrová, O., Horký, P., Slavík, O., Švátora, M., & Petrusek, A. (2017). Feeding habits of the alien brook trout Salvelinus fontinalis and the native brown trout Salmo trutta in Czech mountain streams. Knowledge And Management Of Aquatic Ecosystems, 418, 6. https://doi.org/10.1051/kmae/2016038
- Knapp, R. A., Corn, P. S., & Schindler, D. E. (2001). The Introduction of Nonnative Fish into Wilderness Lakes : Good Intentions, Conflicting Mandates, and Unintended Consequences. Ecosystems, 4(4), 275‑278. https://doi.org/10.1007/s10021-001-0009-0
- Knapp, R. A., & Matthews, K. R. (2000). Non-Native Fish Introductions and the Decline of the Mountain Yellow-Legged Frog from within Protected Areas. Conservation Biology, 14(2), 428‑438. https://doi.org/10.1046/j.1523-1739.2000.99099.x
- Loheac, B.(2020a). Peuplements piscicoles des lacs d’altitude de Savoie : Rapports de synthèse des programmes pluriannuels successifs d’études et de recherche menés par la FDPPMA 73. Volume 3/3. Résultats, analyses et préconisations. FDPPMA 73.
- Loheac, B. (2020b). Peuplements piscicoles des lacs d’altitude de Savoie : Rapports de synthèse des programmes successifs d’étude et de recherche. FDPPMA 73.
- Loheac, B., Caudron, A., & Guillard, J. (2019). Communautés piscicoles introduites des lacs d’altitude : approches scientifiques et influences idéologiques. Revue des Sciences de l’Eau, 32(1), 39‑50. https://doi.org/10.7202/1059879ar
- Mann, R. H. K., Blackburn, J. H., & Beaumont, W. R. C. (1989). The ecology of brown trout Salmo trutta in English chalk streams. Freshwater Biology, 21(1), 57‑70. https://doi.org/10.1111/j.1365-2427.1989.tb01348.x
- Mansoux, H., Martinot, J. P., & Beranger, P. (2020). Les lacs de Savoie : Du Bourget aux lacs nouveaux-nés. Les Pytalierins-Beranger P. Éditions.
- Martinot, J. P. (1978). Acclimatation de l’omble du canada Salvelinus namaycush walbaum (Salmonidae) dans un lac de haute montagne du parc national de la vanoise. Travaux Scientifiques du Parc National de la Vanoise.
- Milardi, M., Siitonen, S., Lappalainen, J., Liljendahl, A., & Weckström, J. (2016). The impact of trout introductions on macro- and micro-invertebrate communities of fishless boreal lakes. Journal Of Paleolimnology, 55(3), 273‑287. https://doi.org/10.1007/s10933-016-9879-1
- Miró, A., O’Brien, D., Tomàs, J., Buchaca, T., Sabás, I., Osorio, V., Lucati, F., Pou-Rovira, Q., & Ventura, M. (2020). Rapid amphibian community recovery following removal of non-native fish from high mountain lakes. Biological Conservation, 251, 108783. https://doi.org/10.1016/j.biocon.2020.108783
- Parnell, A. C., Inger, R., Bearhop, S., & Jackson, A. L. (2010). Source Partitioning Using Stable Isotopes : Coping with Too Much Variation. PLoS ONE, 5(3), e9672. https://doi.org/10.1371/journal.pone.0009672
- Peig, J., & Green, A. J. (2010). The paradigm of body condition : a critical reappraisal of current methods based on mass and length. Functional Ecology, 24(6), 1323‑1332. https://doi.org/10.1111/j.1365-2435.2010.01751.x
- Phillips, D. L., Inger, R., Bearhop, S., Jackson, A. L., Moore, J. W., Parnell, A. C., Semmens, B. X., & Ward, E. J. (2014). Best practices for use of stable isotope mixing models in food-web studies. Canadian Journal Of Zoology, 92(10), 823‑835. https://doi.org/10.1139/cjz-2014-0127
- Steinwandter, M., & Seeber, J. (2023). Ground-dwelling invertebrates of the high alpine : Changes in diversity and community composition along elevation (1500–3000 m). Applied Soil Ecology, 190, 104988. https://doi.org/10.1016/j.apsoil.2023.104988
- Tiberti, R., Von Hardenberg, A., & Bogliani, G. (2014). Ecological impact of introduced fish in high altitude lakes : a case of study from the European Alps. Hydrobiologia, 724(1), 1‑19. https://doi.org/10.1007/s10750-013-1696-1
- Vagnon, C., Pomeranz, J., Loheac, B., Vallat, M., Guillard, J., Raymond, J., Sentis, A., & Frossard, V. (2023a). Changes in vertical and horizontal diversities mediated by the size structure of introduced fish collectively shape food-web stability. Ecology Letters, 26(10), 1752‑1764. https://doi.org/10.1111/ele.14290
- Vagnon, C., Sentis, A., Gerfand, B., Guillard, J., Raymond, J., Loheac, B., Proner, D., Vallat, M., & Frossard, V. (2023b). Persisting in extreme environments : What are the drivers of body conditions of introduced fish in high mountain lakes ? Freshwater Biology, 69(2), 254‑265. https://doi.org/10.1111/fwb.14208
- Ventura, M., Tiberti, R., Buchaca, T., Buñay, D., Sabás, I., & Miró, A. (2017). Why should we preserve fishless high mountain lakes ? Dans J. Catalan, J. Ninot, M. Aniz (dirs), High Mountain Conservation in a Changing World. Advances in Global Change Research (pp. 181-205). Springer. https://doi.org/10.1007/978-3-319-55982-7
Résumé
La capacité des Salmonidés à survivre dans les lacs de montagne reste mal connue et peut orienter leurs politiques de gestion. En se basant sur des données issues de neuf lacs de montagne, nous avons identifié que la condition corporelle des ombles chevaliers (Salvelinus alpinus) ne varie pas significativement avec l’altitude (alt. max. 2 471 m) alors que celles des cristivomers (Salvelinus namaycush) diminue avec l’altitude (alt. max. 2 850 m). L’effet négatif de la profondeur sur les conditions corporelles des cristivomers est contrebalancé par des effets positifs des températures hivernales et des densités en invertébrés littoraux. L’analyse de leurs compositions isotopiques suggère que les deux espèces sont majoritairement soutenues par des ressources aquatiques littorales (moyenne = 67 %). La proportion de ressources terrestres assimilées (6,5 % à 28,9 %) augmente avec l’altitude et diminue avec la superficie et la profondeur traduisant un effet de dilution des proies terrestres avec la taille du milieu. La température estivale des lacs a un effet négatif sur la consommation des ressources terrestres probablement par le biais d’un effet thermique indirect sur la productivité lacustre. Ces résultats permettent de mieux cerner les conditions favorables à la survie des Salmonidés dans ces écosystèmes ainsi que les facteurs influençant leurs alimentations.
Pas de document complémentaire pour cet article
Statistiques de l'article
 Vues: 1
Vues: 1

